“医疗产品的价格是市场容量的决定性的因素。”
“长周期来看,国内原研药物的定价还是会远远低于美国的价格。”
“国家医保局给me-too药物的定价非常的低廉,以PD-1单抗为例,我们统计出来国内的平均定价大概只有美国的4%。”
“长期来看,医保内的产品在国内销售的天花板并不是很高。假如说这些企业想要突破国内医保的天花板,唯一的方法就是把它的产品做成一个全球化的产品。”
“对于非医保产品来说,我们认为它长期的一个方向应该是做成类消费品的产品。”
“传统中成药领域,我们看到它的挖掘的空间越来越有限,后续就要在更加创新的领域去寻找一些消费品化的机会。”
以上是朱雀基金医药组组长周鸣杰12月18日在朱雀基金“赢在终局”2022年度策略会上发表的观点。以下是我们整理的演讲实录。
国际化和消费品化是大方向
首先我想给大家介绍一下创新产品在国内的市场空间。市场容量的公式是量乘以价格。医疗产品的总需求是总人口乘以患病率。人口总数和发病率相对来说是比较稳定的,所以在医疗产品这块量的弹性其实并不是很大,在整个需求量变化不大的前提下,价格就成为市场容量的决定性的因素。
我们来看一下全球各国对创新药物的定价。我们选了4个first-in-class的产品进行价格的比较,first-in-class就是全球创新药物第一家的产品,创新药的皇冠。这4个产品都是通过谈判进入了国家医保的。分析这4个产品在全球4个国家的定价的情况,我们发现以美国作为定价基准,中国的平均定价大概是美国的10%,日本和英国的定价分别是美国的26%和31%。
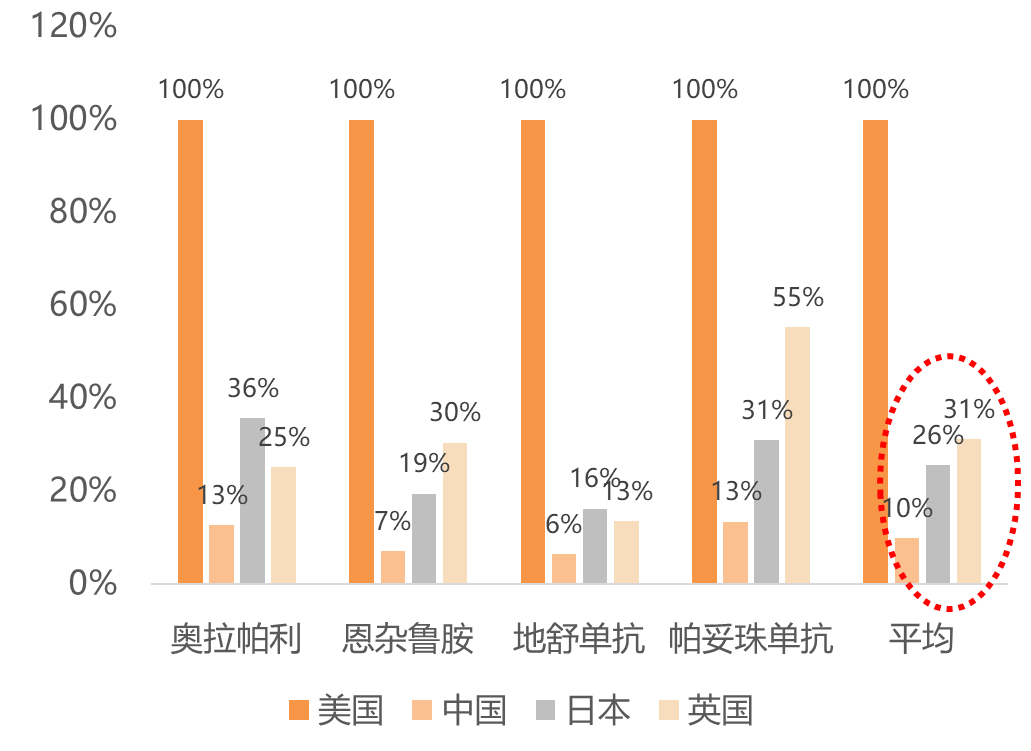
数据来源:国家医保局
我们得到一个结论,中国的原研药物,first-in-class的药物定价比美国低很多。为什么中国的原研药物,first-in-class的药物定价只有美国的10%呢?为什么它的定价这么低?
从常识上来判断,一个药物的定价跟国家的人均医疗支出有关系。所以我们做了一个统计,我们统计了这4个国家的人均卫生总费用,验证了我们前面的猜测。以美国为基准,中国的人均总费用是美国的7%,而日本和英国分别是美国的35%和30%,这个比例和我们前面统计的原研药的定价比例比较接近。
各国2020年人均卫生总费用
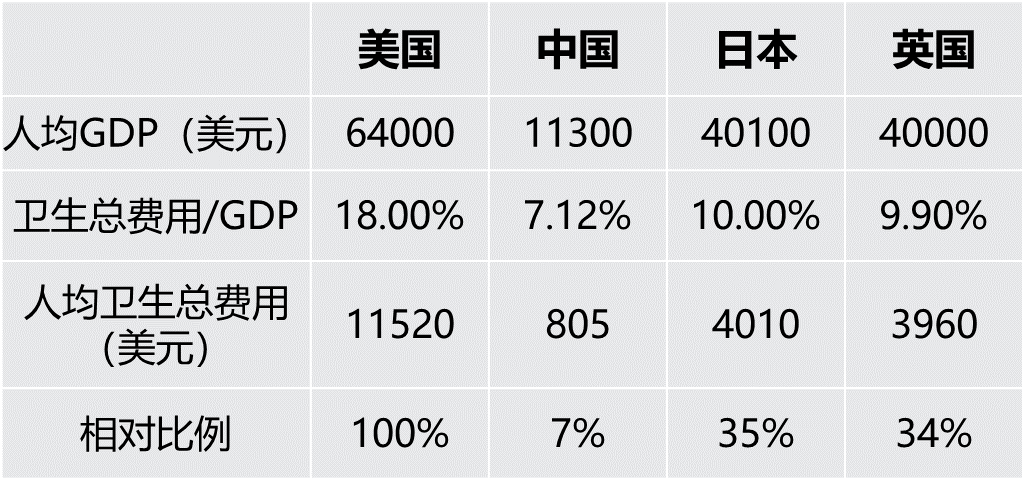
数据来源:世界卫生组织,国家统计局
从统计上我们得到一个结论,各个国家原研药的定价跟它的人均卫生总费用高度相关。在这个结论基础上,我们进一步推演,看一下长期国内的原研药物大概会有怎样的定价。
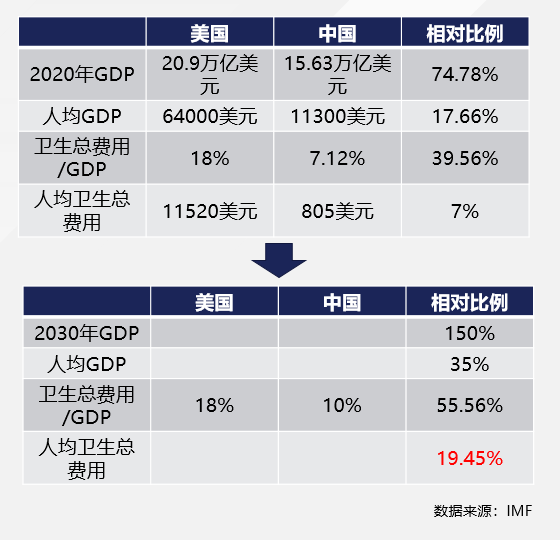
首先我们看一下2020年的情况。前面我们也做了测算,中国的人均卫生总费用是805美元,而美国2020年是11520美元,中国的人均费用大概是美国的7%。我们预测未来,实际上还是要对长期的两个国家的人均卫生总费用做一个推演。
我们假设到2030年的时候,中国的 GDP大概是美国的1.5倍,按照人口不变来测算的话,人均GDP大概是美国的35%。
另外一块就是卫生总费用占GDP的比重,美国在2020年已经达到了18%,这个比例也是全球最高的。那么我们预期到2030年,美国的比重不会再出现比较大幅的上升,会保持平稳。中国的人均卫生总费用除以GDP在2020年只有7.12%,到2030年,我们已经能够达到中等发达国家的平均水平,大概在10%。这样计算下来,我们测算出2030年中国的人均卫生总费用大概是美国的19.4%,也就是接近美国的20%。
根据前面我们的分析来推理,到2030年的时候,中国的原研药物的定价单位接近美国的20%。这个结论代表长周期来看,国内原研药物的定价还是会远远低于美国的价格。
长期来看中美原研药物的定价逻辑
看完了 first-in-class药物的定价情况,我们再来看一下国内现在比较多的me-too药物的定价状况。
国内现在me-too药物实际上面临一个状况,就是内卷非常严重,许多的靶点都有几十家企业在开发me-too的创新药物。实际上国家医保局给这些me-too药物的定价也是非常的低廉,以PD-1单抗为例,国内的平均定价大概只有美国的4%。
从中我们得到一个结论,国内me-too药物的定价比first-in-class的定价更低。根据前面的分析,国内的医疗产品可以大致的分为两类,一类就是在医保内的产品,另外一类就是非医保的产品。医保内的产品如果在国内销售,实际上受到了价格天花板的限制,长期来看,销售天花板并不是很高。假如这些企业想要突破国内的医保天花板,唯一的方法就是把它的产品做成全球化的产品。
对于非医保产品来说,我们认为它长期的方向应该是做成类消费品的产品,才有更大的空间。
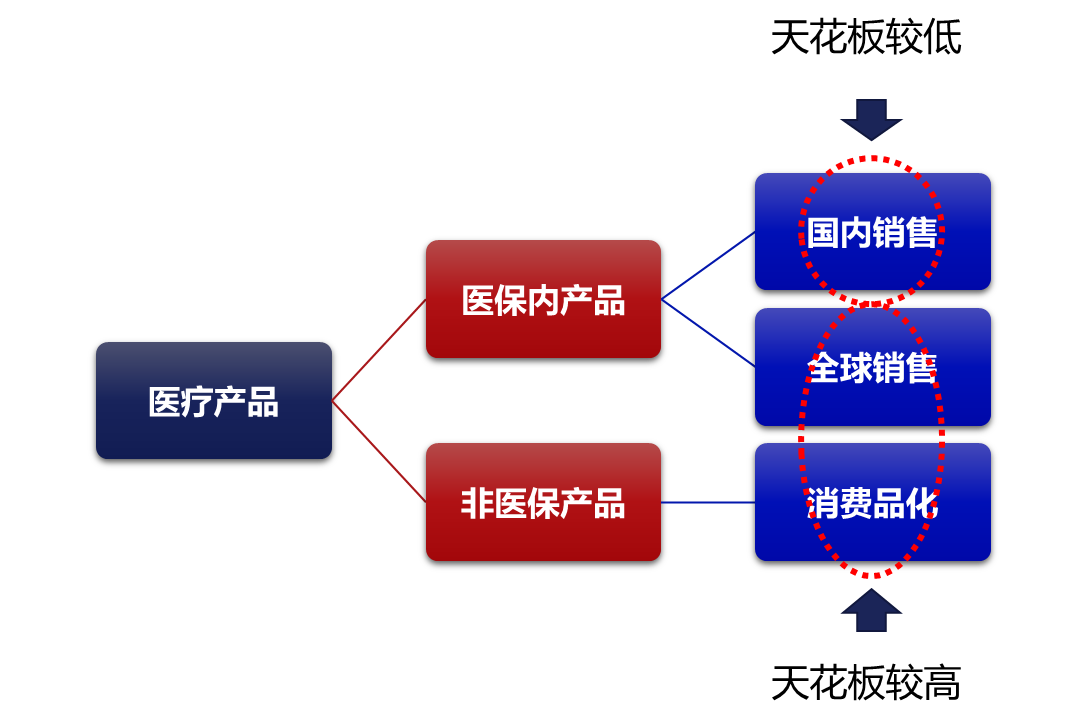
资料来源:朱雀基金整理
医疗企业国际化路径该怎么走
国内制药企业的国际化的路径,我们觉得核心还是在于它的产品要有足够的创新性, 比如first-in-class或 best-in-class的产品。
实现国际化的路径包括三种,第一种是海外授权,第二种是自建海外的销售团队,第三种是直接收购海外的公司。从我们的统计来看,现在全球的制药行业的投资,呈现出一种G2的格局。
越来越多的全球的创新来自于中小型的Start-up企业,它的主要资金来源还是VC/PE,通过观察融资的情况,可以推断出全球创新的活力。
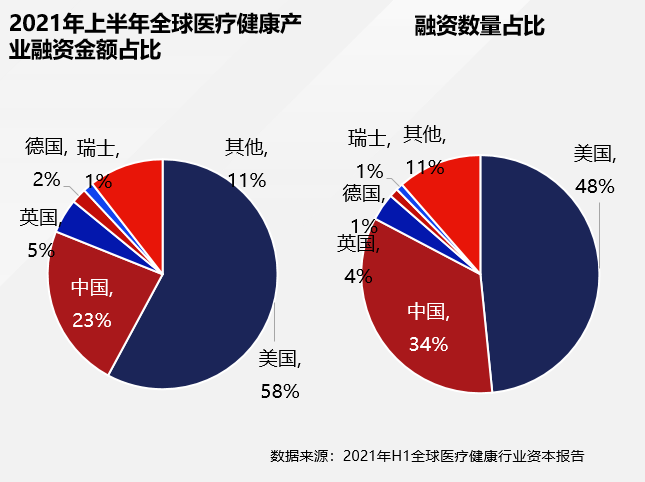
我们统计2021年上半年的全球医疗产业的融资,中国大概占比是23%,美国占比是58%,合计达到了81%。从融资数量来看,中国占比34%,整个融资的格局呈现出一个明显的G2的格局。但是研发创新不仅需要资金上的支持,同样也需要时间上的不断的积累。
中国创新药的全球融资占比是在2015年之后才提升到20%以上,从这个时间的积累来看,往往一个创新药物的创新需要5~10年的时间积累。我们判断从未来5~10年的维度来看,中国的研发创新成果会达到全球比重的20%以上。
另外,我们看到国内制药企业的国际化实际上已经迈出了实质性的步伐。近年来,越来越多的国内企业开始把研发出来的创新药的产品License-out给国外的大型的制造企业。去年最大的一笔交易合计里程碑金额达到了30亿美元,这种30亿美元级别的deal已经在全球处于Top deal的量级。
2020年国内企业License-out前15的项目
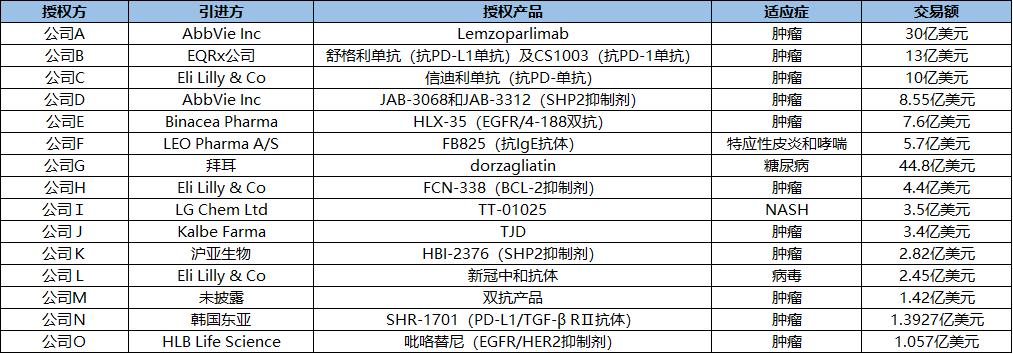
数据来源:朱雀基金整理
我们也观察到一些国内企业开始在美国和欧洲自建销售团队,把自己研发的产品通过销售队伍在美国或者欧洲一些发达国家进行销售。我们相信未来肯定会看到国内的企业通过直接并购的方式去加速国际化的步伐。
我们再来看一下医疗器械的国际化。医疗器械这个品类与制药有很大的不同,在于它的创新更多的是迭代式的微创新,而不是像制药一样呈现出一种颠覆式创新。
疫情期间,中国在中低端耗材领域,比如口罩、手套,已经出现了大量的出口。一些中高端的医疗器械,比如监护仪、制氧机、检验试剂等一些领域,也开始实现出口,一些中国的企业正在做全球创新的产品。
举个例子来说,肥厚性心肌病是心源性死亡的一个重要的原因,占比大概在40%。
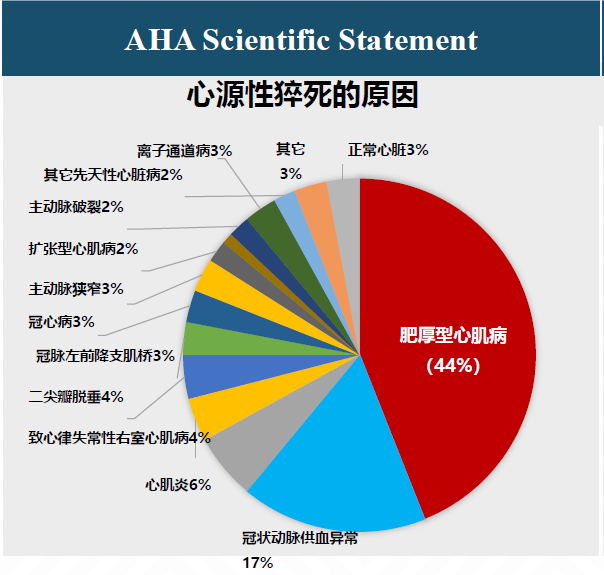
数据来源:启明医疗公司材料
西京医院的刘丽文教授通过多年的临床经验独创出一个Liwen术式,这个术式能够克服传统方式的缺点。这个教授通过跟企业合作的方式,将这个全球创新的治疗方式在美国FDA、欧盟和国内同步开展临床试验。国内实际上有一个很大的优势,就在于病人的数量众多,外科医生由于接触的病人比较多,经验比较丰富。
如果我们能够把转化医学衔接临床和产业的关键做好,未来会有越来越多的在医疗器械领域的全球创新的成果呈现出来。
医疗产品如何实现消费品化
最后是医疗产品的消费品化的优势。
大家比较熟悉的一些中成药,消费品化最成功的企业有两家,一方面这两家企业的产品都是国家绝密的品种,其他人无法仿制。另一方面,他们的品牌在国内消费者中有很高的知名度,节约了大量的广告宣传费用。
在传统中成药领域,挖掘的空间越来越有限,后续要在更加创新的领域去寻找一些消费品化的机会。
创新药的消费品化也有成功案例,比如0.01%的阿托品滴眼液,是一个非常有效的延缓儿童近视的产品。
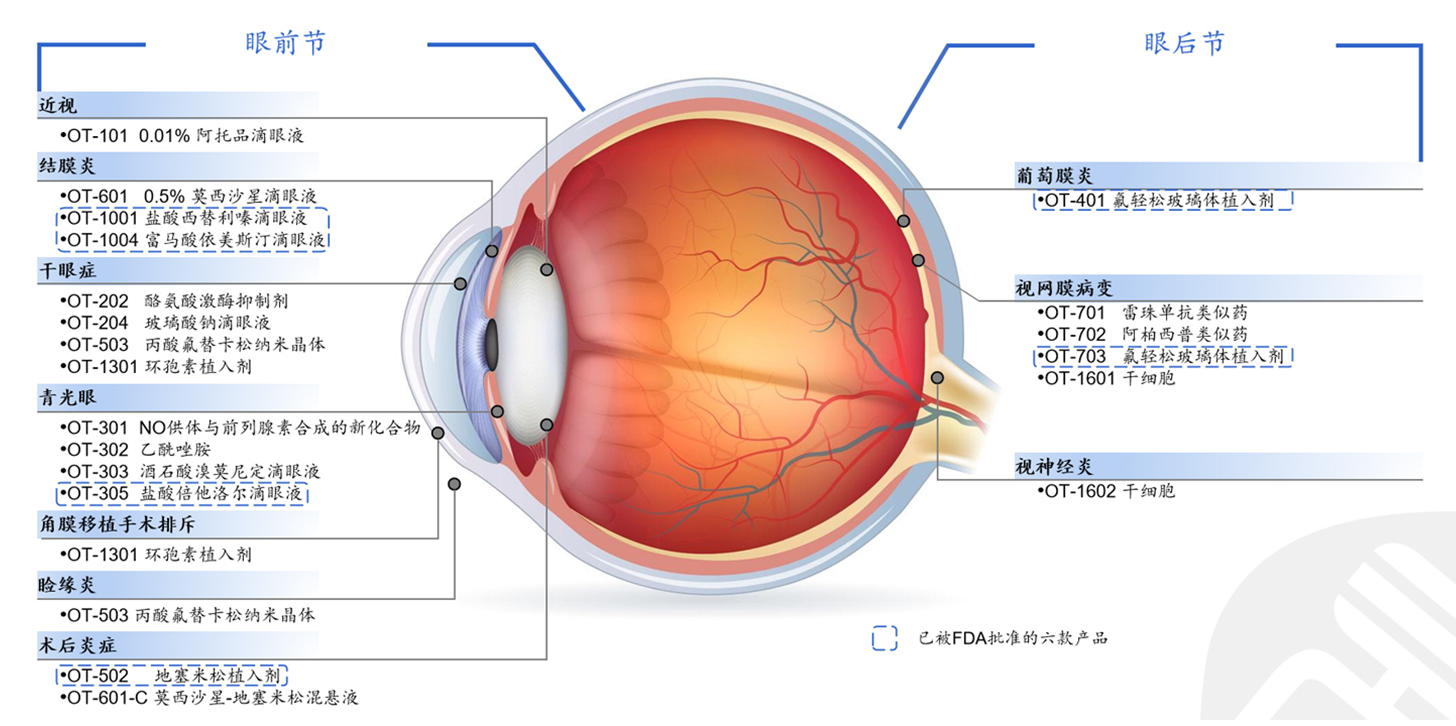
数据来源:欧康维视招股说明书
中国6~18岁的儿童青少年的人口有2亿,近视的比例也超过了50%,它的市场空间是非常大的。家长对儿童用的产品的安全性要求非常高,全球范围内的0.01%的阿托品产品还没有获批上市,首家获批的上市产品将会有巨大的消费品化的优势。
医疗器械消费品化的典型案例是 CGMS(连续血糖监测系统),它可以通过皮下植入,连续监测糖尿病患者或者正常人的血糖变化水平。
与普通的消费产品比,它的优势在于拥有非常高的技术壁垒,全球范围内能够实现CGMS产业化的企业实际上寥寥无几。
另外,血糖监测的准确程度与患糖尿病患者的疾病控制息息相关,与普通消费品相比,患者不会去轻易切换品牌。相对普通消费品来说,我们觉得CGMS这样的医疗器械产品的壁垒更加深厚,消费者粘性更强。
注:本文件非基金宣传推介材料,仅作为本公司旗下基金的客户服务事项之一。
本文件所提供之任何信息仅供阅读者参考,既不构成未来本公司管理之基金进行投资决策之必然依据,亦不构成对阅读者或投资者的任何实质性投资建议或承诺。本公司并不保证本文件所载文字及数据的准确性及完整性,也不对因此导致的任何第三方投资后果承担法律责任。
本文所载的意见仅为本文出具日的观点和判断,在不同时期,朱雀基金可能会发出与本文所载不一致的意见。本文未经朱雀基金书面许可,任何机构和个人不得以任何形式转发、翻版、复制、刊登、发表或引用。